Från provtagning till provsvar
För en bra diagnostik är det viktigt att hanteringen är korrekt hela vägen, från förberedelser inför provtagning till tolkning av provsvar.
Inför provtagning
Provtagningsanvisningar
För att säkerställa rätt förberedelser och provtagning, kontrollera aktuell anvisning bland våra provtagningsanvisingar.
Beställning av provtagningsmaterial
Provtagningsmaterial beställs från Varuförsörjningen. Visst material för använding till patientnära utrustning samt provtagning inför mikrobiologiska undersökningar kan beställas direkt från Laboratoriemedicin. Vi hänvisar då till följande två dokument:
Rekvisitionsblankett för provtagningsmaterial - Klinisk mikrobiologi
Reagens/kontroll beställning PNV
Beställning av analys
Beställning av analys sker i första hand via elektronisk remiss i Cosmic alternativt med pappersremiss. Ytterligare information samt möjlighet att beställa/skriva ut pappersremisser finns under Remisser och etiketter.
Information om rutin- respektive akuta beställningar av analyser finns att läsa i Laboratoriemedicins prislista.
Analyser som kan beställas som akutprov finns i dokumentet Akuta analyser Laboratoriemedicin.
Patientens identitet
ID-kontroll av patienten ska göras innan provtagning, den är viktig för patientsäkerheten och för att undvika provtagning på fel patient.
De regler som gäller för ID-kontroll i Region Västmanland finns i dokumentet Patientidentifikation.
Märkning av provtagningsmaterial
Vilket provtagningsmaterial som ska användas för en given analys finns angivet i aktuell provtagningsanvisning. Kontrollera alltid utgångsdatum på provtagningsmaterialet innan provtagning.
Vakuumrör för venösa prov
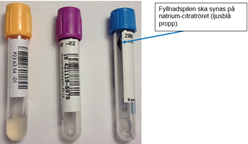
Etiketten ska placeras från proppkanten och längs med röret så att streckkoden kan läsas av maskinellt. På koagulationsröret (Natriumcitratrör med ljusblå propp) ska etiketten sättas så att fyllnadspilen syns, se bild nedan.
Remiss 1-4 med etiketter har unika nummer och får endast användas tillsammans.
Blododlingsflaskor
Blododlingsflaskor hanteras i automatiserade blododlingsskåp, viktigt att Cosmic-etiketten placeras med streckkoden lodrätt på flaskan enligt bild nedan.

Provtagning
Korrekt provtagning är en förutsättning för att kunna få tillförlitliga analysresultat. Det är provtagarens ansvar att försäkra sig om patientens identitet och att uppgifter på remiss/beställning och provtagningsmaterial stämmer överens så att kopplingen till patienten blir korrekt. Provtagningsmaterial ska alltid märkas före provet tas.
Vid provtagning för transfusionsmedicinska undersökningar finns särskilda krav att ta hänsyn till, se information under Transfusionsmedicin.
Venös provtagning
Se information i Vårdhandboken: Blodprov, venös provtagning
Provtagningsrören fylls i rekommenderad rörföljd enligt NCCLS. Se dokument i Region Västmanlands ledningssystem Rörföljd vid venprovtagning.
- Inför provtagning bör patienten vila minst 15 min.
- Använd alltid handskar vid provtagning och hantering av blod.
- Rengör punktionsstället med sprit och låt huden torka ordentligt före instick, för att undvika risk för hemolys.
- Använd så lite stas som möjligt och släpp stasen när blodet börjar rinna.
- Muskelarbete och knuten hand bör undvikas.
- Rör med tillsats skall fyllas tills all vakuumeffekt tar slut. Felaktigt fyllda rör ger felaktiga svar.
- Rören skall, omedelbart efter det att de fyllts, vändas 5 - 10 gånger. Detta gäller även gelrör.
- Vid blodspill på provrörets utsida skall röret avtorkas med alkoholbaserat ytdesinfektionsmedel efter provtagning.
Särskilda instruktioner för provtagning för blododling finns i provtagningsanvisning Blododling vuxna, B- respektive Blododling barn, B-.
Om inget annat anges i Provtagningsanvisningar gäller att blodprov kan förvaras i rumstemperatur om det omhändertas (centrifugeras) inom 4 timmar av laboratoriet.
Kapillär provtagning
Kapillärprovtagning bör i största möjliga utsträckning undvikas. Ett mindre antal analyser kan utföras på kapillärblod. Kapillärprovtagning bör utföras av laboratoriepersonal eller personal särskilt utbildad för detta.
Se information i Vårdhandboken: Blodprov, kapillär provtagning
Rekommenderad rörföljd för kapillärprovtagning
- EDTA-rör
- Rör utan tillsats
- Gel-rör
Provtagning vid infusion
Prov bör alltid tas i en annan extremitet än den där infusionen ges.
Blodprov som tas vid pågående infusion kan vara utspätt med infusionsvätskan i okontrollerad grad och därför rekommenderas att infusionen stängs av innan provtagningen sker. Detta gäller även om prov tas från extremitet där infusionen inte ges. Hur länge man ska vänta med provtagning efter avstängd/avslutad infusion beror på vilken infusion som ges och vilka analyser som ska utföras, samt den enskilde patientens förmåga att omsätta infusionens innehåll. [
Se mer information i Vårdhandboken: Provtagning vid infusion
Lokal anvisning
- För intravaskulära infusioner av röntgenkontrastmedel gäller 10 timmars karenstid innan provtagning
Provtagning ur PVK, CVK eller subkutan venport (SVP)
Se information i Vårdhandboken: Provtagning ur PVK, CVK eller subkutan venport
Lokal anvisning
- Inneliggande kanyl ska inte användas.
- Blodprov får endast i undantagsfall tas ur perifer eller central venkateter och då enbart efter läkarordination. Om provtagning ändå måste ske från inneliggande kanyl, port-A-Cath® eller central venkateter.
- Observera att koagulationsprover aldrig får tas via hepariniserad kanyl/venkateter. Undantag är PICC-line som inte har något heparinlås, vilket gör att koagulationsprover kan tas ur denna kateter.
Hemolys i provrör ger felaktiga provsvar

Orsaker till hemolys
- Långsam provtagning, kombinerat med otillräcklig mängd i röret.
- Nålen ligger inte rätt i venen.
- Ovarsam hantering av röret. Vänd röret varsamt, använd vagga.
- Om provet snabbkyls.
- Huden måste vara torr och fri från rengöringsvätska före provtagning.
- Ej tillräcklig blandning av röret.
- Smala nålar.
- Exempel på hemolyskänsliga analyser: S-ALAT, S-Bilirubin, S-Folat, S-Fosfat, S-Järn, S-LD, S-Kalium, S-Magnesium.
Lumbalpunktion (Csv)
Vid lumbalpunktion ska de rör i vilka cerebrospinalvätska (Csv) samlas numreras i tappningsordning. För rätt sortering ska alla rör lämnas till Jourlaboratoriet, även eventuella rör utan beställning. Se ytterligare information:
Lumbalpunktion-rekommendation för rörföljd och rörantal
Bortskaffande av material
Bortskaffande av material som används i provtagningen hanteras i enlighet med den regionövergripande instruktionen:
Smittförande avfall och skärande/stickande avfall
Se även länk till SOSFS 2005:26 Socialstyrelsens föreskrifter och allmänna råd om hantering av smittförande avfall från hälso- och sjukvården i "Relaterade länkar" ovan.
Centrifugering av prover
Anvisning för mottagningar som själva centrifugerar prover.
Om inget annat anges i respektive provtagningsanvisning gäller att blodprov kan förvaras i rumstemperatur om det omhändertas (centrifugeras) inom 4 timmar av laboratoriet.
Om inget annat anges i respektive provtagningsanvisning ska rören centrifugeras med swing-out rotor vid 2200g (varvtalet beror på centrifugens storlek) i 10 minuter.
Gelrör (serum)
Ska stå upprätt i rumstemperatur minst 30 minuter före centrifugering för att få en god serumseparation.
Om provet inte anländer laboratoriet inom 48 timmar ska serum hällas av i 5 mL plaströr. Undantag finns, se respektive analys.
Rör u t (utan tillsats):
Ska stå upprätt i rumstemperatur minst 60 minuter före centrifugering för att få en god serumseparation.·
Serum överförs, direkt efter centrifugering, med hjälp av pipett till 5 mL plaströr.
EDTA-rör, Na-heparinrör och Citratrör:
Se respektive analys.
Om röret skall centrifugeras, använd pipett för att avskilja plasman till 5 mL plaströr.
Provsvar
Olika analyser och undersökningar tar olika lång tid och svarstiden kan därför variera ganska mycket. Mer information om detta finns ofta i respektive provtagningsanvisning. Beroende på vilket prov det är kan också svaret komma antingen direkt i Cosmic eller i pappersform till beställande enhet.
Resistensbestämning
Resistensbestämning innebär att bakteriers förmåga att överleva i närvaro av olika antibiotika testas. Det ger vägledning om vilket eller vilka antibiotika som kan ha effekt mot en bakterieinfektion och är viktigt för att undvika onödig och felaktig antibiotikabehandling. Resistensbestämning görs även i syfte att övervaka resistensläget.
Resistensbestämningen rapporteras som SIR-kategorisering och/eller MIC (minimal inhibitory concentration). Kategorierna är:
S – Känslig vid normal dosering: En mikroorganism kategoriseras som "känslig vid normal exponering" när sannolikheten för framgångsrik behandling är hög vid normal dosering av medlet.
I – Känslig vid ökad exponering: En mikroorganism kategoriseras som "känslig vid ökad exponering" när sannolikheten för framgångsrik behandling är hög om koncentrationen av medlet i infektionshärden är högre än vid normal dosering. Exponering är en funktion av hur administrationsform, dos, doseringsintervall, infusionstid, distribution och utsöndring påverkar koncentrationen av antibiotika i infektionshärden. Adekvat koncentration av antibiotika i infektionshärden förutsätter adekvat antibiotikadosering, vilket kan kräva dosjustering och/eller förändring av administrationssätt. För råd om dosering kontakta infektionskonsult.
R – Resistent: En mikroorganism kategoriseras som "resistent" när sannolikheten för framgångsrik behandling är låg även vid höga koncentrationer av medlet i infektionshärden.
Brytpunkterna för S, I och R har inrättats så att antibiotika som klassificeras som I är ett lika användbart behandlingsalternativ som antibiotika som klassificeras som S, men kan kräva dosjustering. De antibiotikadoseringar (normaldos respektive högdos) som klassificeringen är baserad på återfinns i NordicASTs brytpunktstabell (www.nordicast.org, flik "dosering").
Tidigare har kategorin I även inkluderat laboratorieteknisk osäkerhet som gjort det svårt att klassificera resultatet som S eller R. Denna sk ATU (area of technical uncertainty) svaras nu ut med en kommentar.
Kontakta gärna Laboratoriemedicins kundservice vid frågor.
Mer information om SIR-definitionerna finns i artikel i läkartidningen (https://www.lakartidningen.se/Klinik-och-vetenskap/Kommentar/2019/01/SIR-systemet-for-att-beskriva-bakteriers-resistens-andras/).
Hänvisning till ackreditering på provsvar
Laboratoriemedicin är ackrediterade enligt SS-EN ISO 15189 för utförande av medicinsk provning. Metoder som omfattas av ackrediteringen framgår på Swedac´s hemsida (Region Västmanland | Swedac), samt av respektive provtagningsanvisning (Provtagningsanvisningar - Region Västmanland (regionvastmanland.se)). På digitala svarsrapporter framgår i dagsläget inte hänvsning till ackreditering via ackrediteringssymbol eller hänvisningstext. Om kund önskar detta, kontaktas Laboratoriemedicin som tillhandahåller svarsrapport i pappersform.
- Skriv ut
-
Länken är kopieradDela texten
- Ändrad den: 1 oktober 2024

